Chemiczny zakątek
by Julia Ruta 2Dp
Spis treści:
Wstęp o chemii
Chemia ( grec. χημεία – chemeia) – nauka badająca naturę i własności substancji , a zwłaszcza przemiany zachodzące pomiędzy nimi. Współcześnie wiadomo, że przemiany substancji wynikają z praw, według których atomy łączą się poprzez wiązania chemiczne w mniej lub bardziej trwałe związki chemiczne , a także praw według których wiązania pękają i tworzą się ponownie prowadząc do przemian jednych związków w drugie co jest nazywane reakcjami chemicznymi . Chemia zajmuje się także rozmaitymi własnościami substancji wynikającymi bezpośrednio z ich budowy atomowej.
Podstawowym zagadnieniem chemii jest badanie substancji i ich przemian jakościowych, powodujących, że z np. z jednej substancji powstają dwie, albo z dwóch jedna. Współczesna chemia stara się wyjaśniać mechanizm tych przemian na poziomie cząsteczkowym. Szuka też zależności między własnościami substancji a ich składem i strukturą atomową.
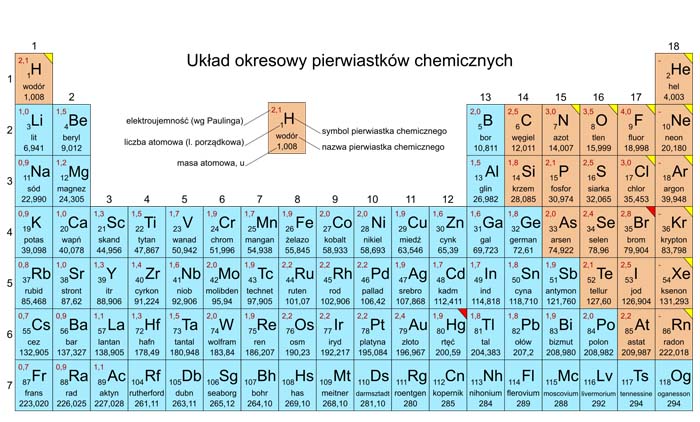
W układzie chemicznym (miejscu gdzie zapisane są wszystkie pierwiastki), wyróżniamy aż 118 substancji zwanych pierwiastkami. My skupimy się jednak tylko na kilku z nich. Do najważniejszych możemy zaliczyć:
W chemii wyróżniamy dwa rodzaje związków chemicznych:
- związki organiczne - muszą zawierać w swoim składzie węgiel. Ponadto znajdują się tam zazwyczaj atomy tlenu, wodoru lub innych pierwiastków.
- związki nieorganiczne - wszystkie związki chemiczne niebędące związkami organicznymi, tj. takie, które nie zawierają atomów węgla oraz nieliczne najprostsze związki węgla tradycyjnie zaliczane do związków nieorganicznych.
Kliknij na mnie!
Znamy już podstawowe pierwiastki, które budują nasz świat. Wiemy też trochę o związkach, które dzięki nim powstają. Ale tak właściwie jak powstaje związek?
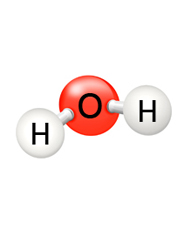
Na rysunku powyżej możemy zauważyć, że 2 atomy wodoru, są połączone z atomem tlenu. Te "połączenia" nazywamy
wiązaniami.
Te z kolei możemy podzielić na kilka rodzaji:
- wiązania jonowe -rodzaj wiązania chemicznego, którego istotą jest elektrostatyczne oddziaływanie między jonami o różnoimiennych ładunkach. Wiązanie to powstaje najczęściej między metalem a niemetalem. Największy udział tego rodzaju wiązania można zaobserwować w związkach litowców z fluorowcami. Teoretycznie najsilniejszym wiązaniem jonowym charakteryzuje się fluorek fransu – FrF, gdyż pierwiastki te mają największą różnicę elektroujemności.
- wiązania kowalencyjne spolaryzowane tworzy się w związkach binarnych – w cząsteczkach heteroatomowych, np.: HCl, H2O, NH3, CH4, CO2. Dla tych przykładów różnica elektroujemności jest większa od 0 i mniejsza od 1,7;
- wiązania kowalencyjne niespolaryzowane -tworzy się między dwoma jednakowymi atomami, czyli przede wszystkim w cząsteczkach homoatomowych typu X2: H2, N2, O2, F2, Cl2, Br2, I2. Dla każdego z tych przykładów różnica elektroujemności jest równa 0,
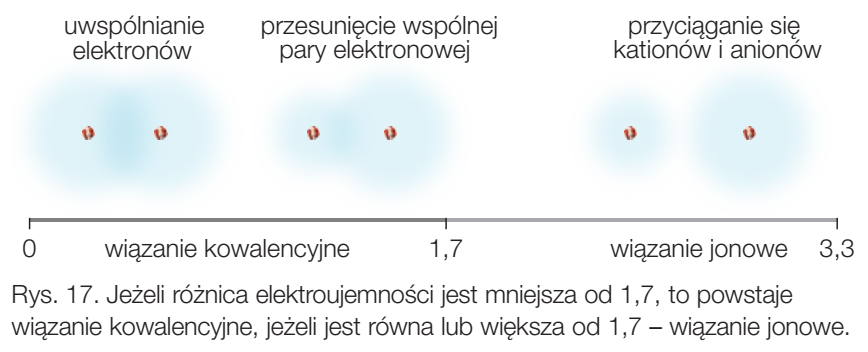
Wiązania między pierwiastkami

Nauka, nauką, ale czy chemia to tylko ścisła teoria i nuda? Otóż nie! Przed wami kilka interesujących informacji, o których mogliście nie wiedzieć, a również dotyczą chemii:
- Węgiel ma miliony różnych zastosowań - od węglowodoru używanego w benzynie po polimer używany do produkcji plastiku. Ale jedna mała rzecz wydaje się dość niesamowita: z węgla znajdującego się w twoim ciele możesz zrobić prawie 10 000 ołówków!
- Kolor fajerwerków jest uzależniony od materiałów, których dodaje się do nich przy produkcji. I dlatego za kolor żółty odpowiadają sole sodu, za czerwony – sole litu, różowy – rubid, zielony – miedzi, fioletowy – potasu, niebieski – cezu.
- Gal, który jest pierwiastkiem metalicznym, o liczbie atomowej 31, roztopiłby się w naszej dłoni. Dzieje się tak, bowiem temperatura jego topnienia, to zaledwie 29, 8 C.
Do najsłynniejszych chemików, którzy zmienili już na zawsze nasz świat, możemy zaliczyć:
pomysł oraz wykonanie - Julia Ruta klasa 2Dp